*仅供医学专业人士阅读参考百进配资
糖尿病患者常伴有糖脂代谢紊乱。据调查,我国2型糖尿病(T2DM)患者中超重比例为41%,肥胖比例为24.3%,而腹型肥胖患者高达45.4%[1]。此外,T2DM患者中有高达59.36%合并有非酒精性脂肪肝(NAFLD),控制不佳、肥胖和女性患者面临更高风险[2]。一方面,T2DM会加速NAFLD的病情进展,使其逐渐发展成为非酒精性脂肪性肝炎(NASH)、肝纤维化、肝细胞癌等;另一方面,NAFLD也会给T2DM的管理带来不利,加重胰岛素抵抗,加重糖脂代谢紊乱,使心血管疾病的发生风险增加[3],从而给糖尿病的综合管理带来挑战。
聚乙二醇洛塞那肽(以下简称洛塞那肽)是我国自主研发的首个GLP-1RA周制剂,近年来的一些临床研究证实了其能够带来降糖、降脂、减重、保护肝脏及等多种获益,有助改善T2DM患者的代谢紊乱。本文将对相关研究证据进行回顾和总结。
针对肥胖T2DM患者的临床研究证实洛塞那肽能够显著降脂并减重
一项开放随机对照试验纳入156例超重/肥胖的T2DM患者(BMI≥25kg/m2),随机2:1分为洛塞那肽(0.3mg)组和二甲双胍(1500mg)组,评估对患者体重的短期影响。治疗16周后发现,洛塞那肽组体重下降7.52kg,减重效果是二甲双胍(下降2.96kg)的2.5倍,且使61.5%的患者实现了≥5%的临床意义减重(P<0.001)(图1)[4]。
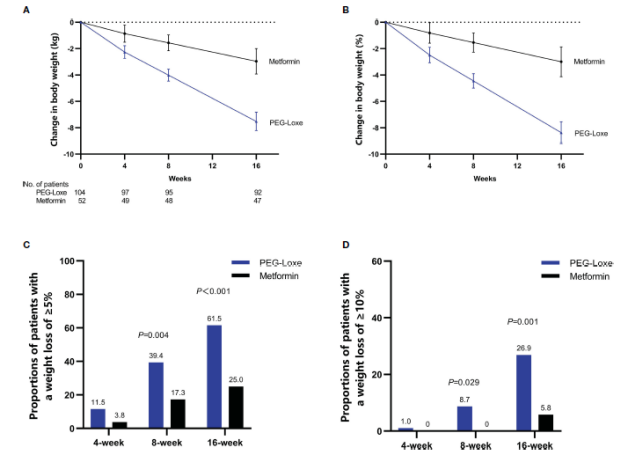
图1.治疗16周期间两组的体重变化[4]
该研究还发现,相比二甲双胍,洛塞那肽能够显著改善总胆固醇(TC)、甘油三酯(TG)和胆固醇(LDL-C)脂代谢指标(P<0.001),并减少内脏脂肪面积(VFA)(-26.02cm2 vs -12.39cm2,P<0.001)[4]。
另一项随机研究纳入40例合并肥胖的T2DM患者(BMI≥28kg/m2),比较二甲双胍(1500~2000mg/日)联合洛塞那肽(起始剂量0.1mg,每周1次)(研究组)相比二甲双胍单药(1500~2000mg/日)(对照组)对血脂、血糖及体重的影响[5]。
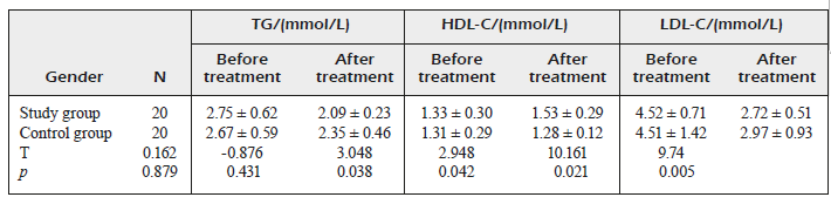
结果发现,研究组患者的体重和BMI自治疗1个月后不断降低,治疗7个月以上的体重和BMI下降最明显:从治疗1个月时的平均76.25kg下降至平均58.13kg,BMI从平均28.19kg/m2下降至21.46kg/m2(P<0.05),而对照组无明显变化(P>0.05)[5]。治疗后,研究组TG和LDL-C水平显著低于对照组(P<0.05),而高密度脂蛋白胆固醇(HDL-C)水平则显著高于对照组(P<0.05)(表1)[5]。
表1.两组治疗前后脂质水平的比较(n, x±s)[5]
临床和基础研究证实洛塞那肽有助改善脂肪肝并保护肝脏
一项研究纳入90例肥胖T2DM患者,随机2:1分为洛塞那肽组(0.2mg,每周1次)和二甲双胍组(0.5g,每日3次),旨在探讨洛塞那肽对此类患者体重、腰围和内脏脂肪面积(VFA)的影响。结果显示,治疗8周后,相比二甲双胍,洛塞那肽组体重、腰围、BMI、VFA的降幅均更为明显(P均<0.05)。其中,洛塞那肽组体重下降了5kg,二甲双胍组仅下降0.6kg;洛塞那肽组VFA减少20.5cm2,而二甲双胍组仅减少3cm2[6]。
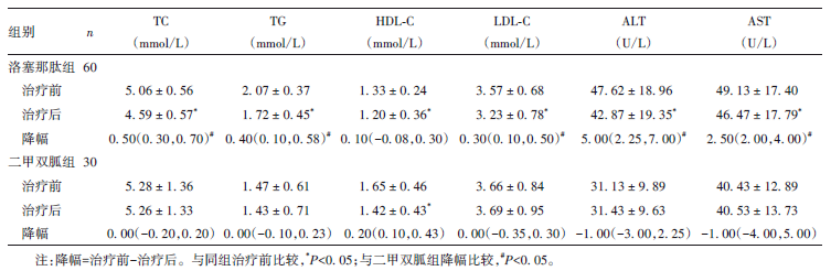
此外,洛塞那肽组脂代谢指标(TC、TG、LDL-C)和肝功能指标(ALT、AST)降幅也较二甲双胍组更明显(P<0.05),提示洛塞那肽有效减脂的同时,还具有一定的肝保护作用(表2)[6]。
表2.两组治疗前后血脂、肝功能比较[6]
一项动物模型实验也证实了洛塞那肽的肝脏保护作用。该研究发现洛塞那肽能够通过降低肝脏TG、TC水平及减少脂滴沉积而改善脂肪肝,其能够通过上调Sirt1/AMPK信号通路、下调FAT/CD36而促进脂肪酸氧化,抑制脂质合成(图2)[7]。
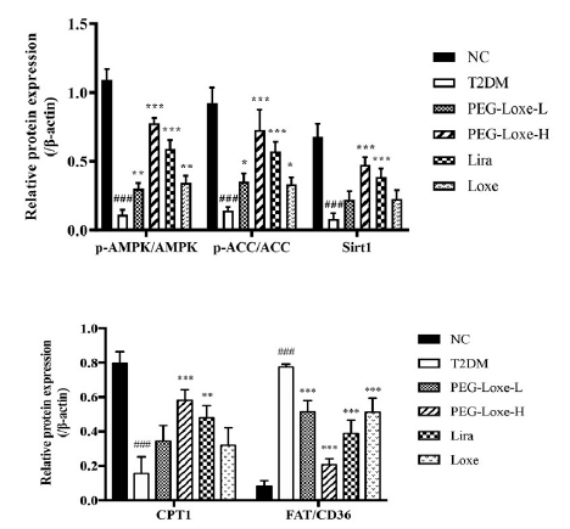
图2.洛塞那肽对Sirt1-AMPK信号通路的影响[7]百进配资
最新机制研究首次阐明洛塞那肽通过调控SRA/CNBP/ROCK2轴改善胰岛素抵抗和脂质代谢紊乱[8]
《糖尿病研究杂志》(Journal of Diabetes Investigation)的一项研究采用T2DM大鼠模型,将其分为对照组、模型组、低剂量和高剂量洛塞那肽组。结果发现:
洛塞那肽显著改善胰岛素抵抗
高剂量洛塞那肽显著降低T2DM大鼠的空腹血糖(FBG)、口服糖耐量试验(OGTT)曲线下面积(AUC)及空腹胰岛素水平(FINS),并降低HOMA-IR指数,同时提升HOMA-IS指数。低剂量组则对上述指标的改善作用较弱,提示疗效呈剂量依赖性。
洛塞那肽纠正脂质代谢紊乱
组织病理显示,高剂量洛塞那肽显著减轻T2DM大鼠的肝脏脂肪变性,降低肝组织中脂肪酶I(LIPI)蛋白表达。高剂量洛塞那肽还可显著降低T2DM大鼠血清和肝脏中的TG、TC,降低血清瘦素(Leptin)水平,并升高脂联素水平。
洛塞那肽抑制炎症与氧化应激
洛塞那肽以剂量依赖性方式下调T2DM大鼠肝脏活性氧(ROS)水平,下调促炎因子(TNF-α、IL-1β、IL-6),上调抗炎因子IL-10水平。
洛塞那肽通过调控SRA/CNBP/ROCK2轴改善T2DM
洛塞那肽显著下调T2DM大鼠肝脏中SRA的表达,且SRA过表达可逆转洛塞那肽的保护作用。SRA与CNBP共同增强ROCK2 mRNA稳定性,促进RhoA/ROCK2信号通路激活。而高剂量洛塞那肽可抑制该通路,降低ROCK2蛋白表达及活性,从而改善胰岛素抵抗和脂代谢紊乱(图3)。
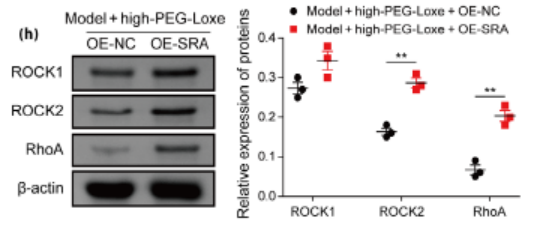
图3.高剂量洛塞那肽抑制SRA过表达引起的RhoA/ROCK2信号通路激活
本研究首次阐明洛塞那肽通过调控SRA/CNBP/ROCK2轴改善T2DM的分子机制。SRA与RhoA/ROCK2通路的关联机制不仅限于糖尿病,还可能为NAFLD、肥胖等代谢性疾病的治疗研究提供新思路。
大型真实世界研究证实洛塞那肽显著降低心血管事件风险[9]
已知血脂水平与心血管疾病风险之间存在明确、直接且强烈的因果关系,因此血脂的良好管理有助于降低心血管疾病风险。MedComm发表的一项大型多中心双向队列研究(FLYING研究),为洛塞那肽的心血管获益提供了确凿的真实世界证据。
该研究对12341例具有心血管疾病或心血管危险因素的T2DM患者进行了回顾性筛查百进配资,比较了接受洛塞那肽(治疗组)和接受非肠促胰岛素类降糖药治疗(对照组)的患者,在长期随访4年后的心血管不良事件发生率(图4)。
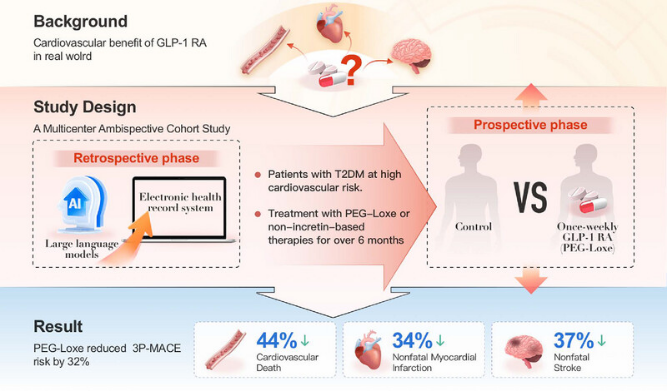
图4.FLYING研究简介
结果发现,洛塞那肽组患者相比对照组的主要心血管不良事件风险下降32%,且首次非致死性心肌梗死、非致死性卒中及心血管死亡的发生率均明显更低,风险分别下降34%、37%和44%(图5)。
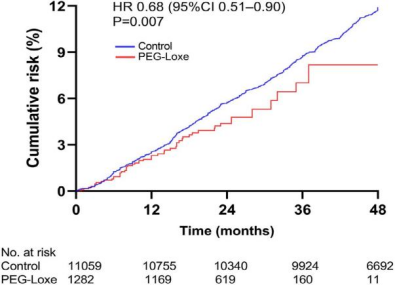
图5.三终点主要不良心血管事件(3P-MACE)的累积发生率
结语
现有的临床及基础研究证据表明,洛塞那肽具有超越传统降糖药物的降脂、减重、肝保护、心血管保护等综合代谢改善优势。对于合并超重/肥胖的T2DM患者,洛塞那肽能够有效减少内脏脂肪、缩小腰围并改善体重,还能够优化血脂水平以降低血脂紊乱带来的潜在代谢及心血管疾病风险。洛塞那肽还能够通过降低肝脏TG、TC水平及减少脂滴沉积而改善脂肪肝,且可通过改善ALT/AST指标而保护肝脏。最新研究还揭示其通过阻断SRA/CNBP/ROCK2轴,从源头改善胰岛素抵抗和代谢紊乱。大型真实世界研究证实了洛塞那肽长期治疗具有心血管保护作用,可显著降低心血管不良事件风险。总之,洛塞那肽具有除降糖以外的额外代谢获益,有助于糖尿病患者的综合管理。
专家简介

姜强
济南市中心医院东院区内分泌与代谢病科 主任医师
山东省健康管理协会泛血管疾病(肥胖与代谢病管理)专业委员会 副主任委员
山东免疫学会干细胞与免疫专委会副主任委员
济南医学会内分泌专业委员会副主任委员
山东预防医学会糖尿病防治分会常务委员
山东省医学会糖尿病足与慢性创面多学科联合委员会委员
山东省老年医学会内分泌分会委员
山东省干细胞学会创伤修复与组织再生专业委员会委员
长期从事临床内科工作,擅长糖尿病、甲状腺机能异常、痛风、肾上腺相关疾病、骨质疏松、性发育异常、更年期综合征等内分泌代谢疾病的诊治,研究方向:糖调节异常的筛查及早期干预,糖尿病并发症的防治,难治性高血压,难治性甲亢的治疗
参考文献:
[1].中华医学会内分泌学分会. 中国2型糖尿病合并肥胖综合管理专家共识[J]. 中华内分泌代谢杂志,2016,32(8):623-627.[2].Han X, Zhang X, Liu Z, Fan H, Guo C, Wang H, Gu Y, Zhang T. Prevalence of nonalcoholic fatty liver disease and liver cirrhosis in Chinese adults with type 2 diabetes mellitus. J Diabetes. 2024 May;16(5):e13564.[3].中华医学会内分泌学分会,中华医学会糖尿病学分会. 中国成人2型糖尿病合并非酒精性脂肪性肝病管理专家共识[J]. 中华内分泌代谢杂志,2021,37(7):589-598.[4].Cai H, Chen Q, Duan Y, Zhao Y, Zhang X. Short-term effect of polyethylene glycol loxenatide on weight loss in overweight or obese patients with type 2 diabetes: An open-label, parallel-arm, randomized, metformin-controlled trial. Front Endocrinol (Lausanne). 2023 Jan 26;14:1106868.[5].Li XY, Li CP, Zhang CY, Zhang S, Chen JX, Zhu D, Chen FW, Wu ZZ, Hou DC, Zheng CY, Hou KJ. Effect of polyethylene Glycol Loxenatide (long-acting GLP-1RA) on lipid, glucose levels and weight in type 2 diabetes mellitus patients with obesity. Eur Rev Med Pharmacol Sci. 2022 Nov;26(21):7996-8003.[6].王燕,张秀娟. 聚乙二醇洛塞那肽对肥胖2型糖尿病患者体质量、腰围和内脏脂肪面积的影响[J]. 山东医药,2022,62(25):35-38.[7].Zhang Y, Li Y, Zhao J, Wang C, Deng B, Zhang Q, Shi C. Protective Effects and Mechanisms of Polyethylene Glycol Loxenatide Against Hyperglycemia and Liver Injury in db/db diabetic Mice. Front Pharmacol. 2021 Dec 6;12:781856.[8].Chen Z, Zhou Z, Wang L, Zhang Y, Huang C, Wang C, Huang Y, Wang S, Yan D, Feng K. Polyethylene glycol loxenatide modulates lipid metabolism and insulin resistance through lncRNA steroid receptor RNA activator/cellular nucleic acid binding protein/Rho-associated coiled-coil kinase 2 axis in type 2 diabetes mellitus. J Diabetes Investig. 2025 Apr;16(4):715-727.[9].Li J, Tian Y, Li L, Zhao Y, Yang S, Xu W, Zhu D, Ye J, Chen J, Liu W, Xue H, Wu W, Deng F, Duan Y, Hu Z, Xie B, Chen ZS, Hou K. Once-weekly glucagon-like peptide receptor agonist polyethylene glycol loxenatide protects against major adverse cardiovascular events in patients with type 2 diabetes: a multicenter ambispective cohort study (FLYING trial). MedComm (2020). 2025 Feb 13;6(2):e70094.
“此文仅用于向医疗卫生专业人士提供科学信息,不代表平台立场”
俊升配资提示:文章来自网络,不代表本站观点。